(第8版第7刷:2025年2月20日発行)
正誤表
この度は,上記書籍をご購入くださいまして誠にありがとうございました.
以下の箇所に関して誤りがございましたので,ここに訂正するとともに深くお詫び申し上げます.
2025年6月30日更新
| 頁 | 箇所 | 誤 | 正 |
|---|---|---|---|
| 228 | 左段 下から8行目 | 麻酔器に供給されるように | 麻酔器に供給されないように |
|
■2020年心肺蘇生法ガイドライン(第15章 心肺蘇生法 補遺)
2021年7月12日に日本の心肺蘇生法ガイドラインが変更された.2020年ガイドラインなのでG2020と呼ばれる.『歯科麻酔学』第8版第4刷は最新のG2020に改訂済みであるが,以下,一部補足する. (佐久間 泰司) |
|
■新型コロナウイルス感染症対応の救急蘇生法(第15章 心肺蘇生法 補遺)
1.はじめに (佐久間 泰司)
文献 |
(第8版第3刷:2021年2月20日発行)
正誤表
この度は,上記書籍をご購入下さいまして誠にありがとうございました.
以下の箇所に関して誤りがございましたので,ここに訂正するとともに深くお詫び申し上げます.
2021年3月8日更新
| 頁 | 行 | 誤 | 正 |
|---|---|---|---|
| 182 | 左段17行目 | プレフィルドシリンジとして500mL中に200μg | プレフィルドシリンジとして50mL中に200μg |
補足情報
2021年4月6日更新
|
■2020年心肺蘇生法ガイドライン(第15章 心肺蘇生法 補遺)
2020年3月末に日本の救急蘇生ガイドラインが変更された. (佐久間 泰司)
文献 |
|
■新型コロナウイルス感染症対応の救急蘇生法(第15章 心肺蘇生法 補遺)
1.はじめに (佐久間 泰司)
文献 |
(第8版第2刷:2020年2月20日発行)
正誤表
この度は,上記書籍をご購入下さいまして誠にありがとうございました.
以下の箇所に関して誤りがございましたので,ここに訂正するとともに深くお詫び申し上げます.
2021年3月25日更新
| 頁 | 行 | 誤 | 正 |
|---|---|---|---|
| 124 | 左段20行目 | 600 mg 以上の投与でメトヘモグロビン血症を起こす. | メトヘモグロビン血症の患者には禁忌である. |
| 128 | 右段6行目 | フェリプレシン含有% | フェリプレシン含有3% |
| 131 | 左段7行目 | α1C | α1D |
| 142 | 左段3行目 | 眼窩下溝 | 眼窩下孔 |
| 177 | 左段下から2,5行目 | 急性狭隅角緑内障患者 | 急性閉塞隅角緑内障患者 |
| 280 | 右段下から5行目 | ②PVC | ②PCV |
| 286 | 左段2行目 | 不整脈にはリドカインを投与し | 不整脈にはCa拮抗薬以外の抗不整脈薬を投与し |
| 329 | 表6-Ⅱ-3 収縮期血圧(mmHg)列 | 140 ≧/135 ≧/130 ≧/135 ≧/120 ≧ | ≧140/≧135/≧130/≧135/≧120 |
| 351 | 左段下から15行目 | 上限と下限ともに右方移動している.高血圧患者,~ | 上限と下限(平均動脈圧の25%の低下)ともに右方移動している.神経生理学的機能不全や障害を予防するためには,高血圧患者,~ |
| 362 | 左段1行目 | これらの治療薬は | 抗甲状腺薬やヨードは |
| 407 | 右段5行目,12行目 | Le Fort 型骨切り術 | Le Fort Ⅰ型骨切り術 |
| 412 | 左段5行目 | 生後~4か月 | 生後3~4か月 |
(第8版第1刷:2019年2月20日発行)
正誤表
この度は,上記書籍をご購入下さいまして誠にありがとうございました.
以下の箇所に関して誤りがございましたので,ここに訂正するとともに深くお詫び申し上げます.
2020年2月27日更新
| 頁 | 行 | 誤 | 正 |
|---|---|---|---|
| 11 | 表1-Ⅱ-2 | ・・・第93回2015 年 ボストン(会長:山崎信也).毎年開催. | ・・・第93回2015 年 ボストン(会長:山崎信也).第95回2017 年 サンフランシスコ(会長:藤澤俊明).毎年開催. |
| 102 | 右段 20行目~ | 排卵期は低く黄体期は高くなる(0.3~0.5℃) | 月経前期は低く月経後期(排卵日から次の月経開始までの黄体期)は高くなる(0.3~0.5℃) |
| 139 | 表3-Ⅳ-3 文献番号 | ( 金子,199657)より改変) | ( 金子,199658)より改変) |
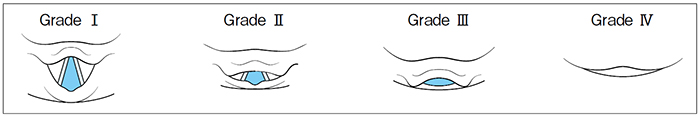
| 204 | 右段 19行目 | 表5-Ⅲ-1に気道確保に関する術前評価項目を示す(図5-Ⅲ-1). | 表5-Ⅲ-1に気道確保に関する術前評価項目を示す(図5-Ⅲ-1).また,気管挿管の難易度の評価には,直視型喉頭鏡(Macintosh型)のブレードによる喉頭展開時の視認度を基準とした Cormack & Lehane 分類(C-L分類)も用いられている(図5-Ⅲ-2). |
| 205 | 図5-Ⅲ-2 を追加 |
|
|
| 420 | 左段 下から7行目 | 小児では輪状軟骨部であり, | 小児では輪状軟骨部(声門下との報告もある)であり, |
| 474 | 左列 下から1行目 | 異常感覚,錯感覚,知覚過敏,知覚鈍麻,無感覚など | 異常感覚,錯感覚,感覚過敏,感覚鈍麻,無感覚など |
| 476 | 左列 16行目~ | 神経中脳路核を通って,延髄,中脳,視床,そして大脳知覚野と連絡される.末梢神経障害の原因が特定できない場合や広範囲で多様な症状を呈する場合,三叉神経節より上位中枢の障害の可能性がある.その原因には,脳腫瘍や多発性硬化症がある. | 神経中脳路核を通って,視床そして大脳と連絡される.末梢神経障害の原因が特定できない場合や広範囲で多様な症状を呈する場合,上位中枢の障害の可能性がある.その原因には,脳腫瘍や多発性硬化症がある. |
| 476 | 左段 下から15行目 | 2.末梢性三叉神経感覚障害(三叉神経ニューロパチー) | 2.末梢性三叉神経感覚障害(外傷性三叉神経ニューロパチー) |
| 476 | 左段 下から11行目 | 知覚鈍麻 | 感覚鈍麻 |
| 477 | 右段 9行目 | 知覚鈍麻 | 感覚鈍麻 |
| 478 | 図12-Ⅳ-4 |
【誤】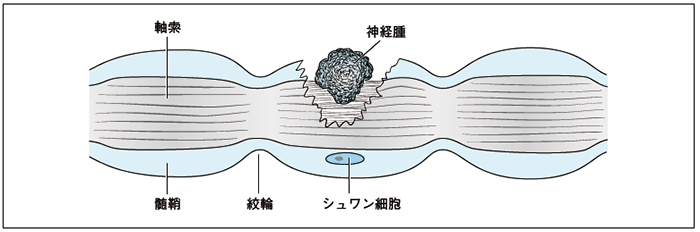 【正】 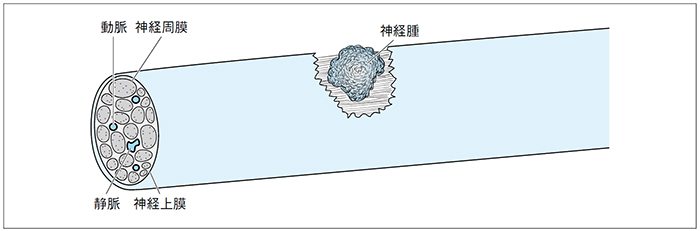
|
|
| 478 | 図12-Ⅳ-5 |
【誤】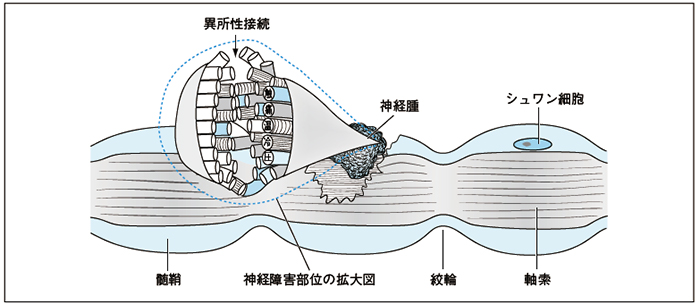 【正】 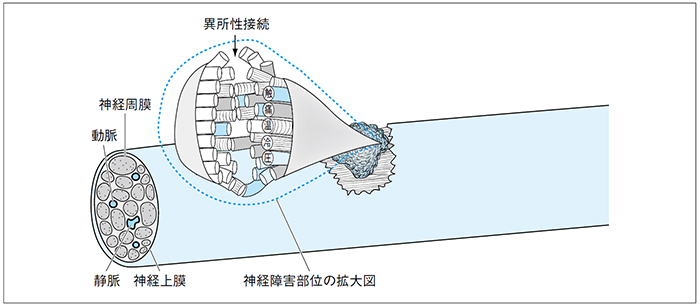
|
|
| 478 | 左段 下から2行目 | 知覚鈍麻 | 感覚鈍麻 |
| 479 | 左段 1,8,21行目 右段 1,16行目 |
知覚鈍麻 | 感覚鈍麻 |
| 513 | 表13-Ⅱ-1 ブリックテスト |
上腕の腹側の皮膚に薬液をおいて,23~26G の針を用いて,皮膚に対してベベルを45度にし,皮膚が持ち上がる程度の深さで刺す.薬液は希釈しないものを用いる.15~30 分後に判定し,5 mm 以上の膨疹,または10 mm 以上の発赤で陽性とする. | 前腕の掌側皮膚にプリックテスト専用針であるバイファーケイテッドニードル(東京エム・アイ商会)を用いて,小さな穴を開けた後,局所麻酔薬の原液を滴下する.判定は15~20分後に行い,膨疹の直径がnegative controlより3mm大きいか,あるいはpositive controlの半分以上の場合を陽性とする. |
| 513 | 表13-Ⅱ-1 皮内テスト(intradermal test: IDT) |
テスト用診断液(100倍希釈)0.1 mLを皮内に注射し,1~2mmの膨疹をつくる.15~20 分後に判定する.10 mm 以上の持続性の膨疹,または20 mm以上の発赤で陽性と判定する.生理食塩液によるnegative controlと0.01%ヒスタミン溶液によるpositive controlとの比較も必要である.IDTの陽性率は60~70%であり,偽陽性率は10~15%にも達する.IDTの臨床的意義が疑問視されている. | 10倍に希釈した局所麻酔薬0.02~0.05mlを真皮内に注入し,直径4mmまでの膨疹を作る.注入20分後の紅斑性の膨疹(しばしば掻痒性)の直径が薬剤注入後と同等から2倍以上の大きさであれば陽性とする. |
| 513 | 表13-Ⅱ-1 補注として表下に追加 |
- | 生食をnegative control,10mg/mLヒスタミン二塩酸塩を1000倍に希釈した溶液をpositive controlとして用いる. |
| 514 | 左段 2~12行目 | in vitroの検査には,Ⅰ型アレルギー反応を調べる検査として,アレルゲン特異的IgE 抗体の測定や抗原刺激による好塩基球からのヒスタミン遊離を測定するヒスタミン試験(HRT)がある.また,Ⅳ型アレルギー反応をみるリンパ球幼若化試験(LST)などがあり,局所麻酔薬のアレルギー診断にも用いられる.しかし,これらの検査が皮膚テストやチャレンジテストの結果と一致するとは限らない.したがって,アレルギー診断は複数の検査から総合的に行う必要がある. | in vivo検査には,Ⅰ型アレルギーを調べる検査として,好塩基球活性化試験(basophil activation test: BAT)がある.Ⅰ型アレルギーでは,マスト細胞と同様に好塩基球細胞も活性化される.マスト細胞は血液中に存在しないため,同様の反応を示す末梢血中の好塩基球をターゲットとする.アレルギー反応を患者自身の細胞で直接とらえるため,臨床症状との一致性が高いとされている.アナフィラキシーショックなどのハイリスク症例で,生体内(in vitro)試験を行わずに抗原診断を行うための補助検査として有用である.BATでは,検査したい抗原を任意に選択できる利点がある. Ⅳ型アレルギーを調べる検査として,薬物によるリンパ球刺激試験(drug-induced lymphocyte stimulation test: DLST)と白血球遊走試験(leucocyte migration test: LMT)があるが,原因薬剤の検出率は低く,偽陽性も多い. in vitro試験の結果が,皮膚テストやチャレンジテストの結果と一致するとは限らない.アレルギー診断では,何種類かの検査を組み合わせ,臨床症状も加味して,総合的にアレルギーの有無を判断する必要がある. |